Българската система за верификация на лекарствата вече е свързана с Европейския хъб
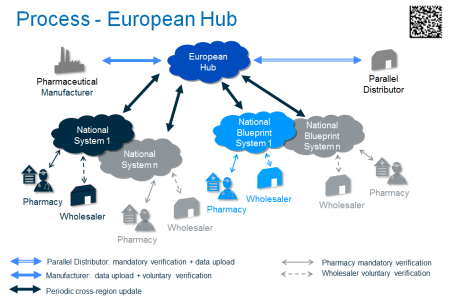
GS1 България информира, че на 18 април 2018 г. Българската система за верификация на лекарствата (БСВЛ) беше свързана с производствената среда на Европейския център (EU Hub). С това успешно бе изпълнена една от най-важните цели на Българската организация по верификация на лекарствата, БОВЛ, България да бъде в първата вълна от Blueprint системи, интегрирани с Европейския център и работещи в реална среда. Постигането на тази цел стана възможно благодарение на отличното сътрудничество, професионализъм и ангажираност на членовете на борда на БОВЛ, екипа на Solidsoft Reply, Европейската организация за верификация на лекарствата (EMVO), Словенската медицинска организация за верификация (MVIS – ZAPAZ), национални организации за верификация на лекарствата от други страни и всички консултанти и компетентните органи, ангажирани в проекта през изминалите две години.
Заедно със свързването стартира и тестване на пилотни участници за връзка с Европейския център и с Националната система. Изпълнението на цитираните по-горе дейности по график осигурява достатъчно време на всички участници по веригата за снабдяване с лекарства за свързване, тестване, обучение и своевременна подготовка. Това позволява внедряване на системата без напрежение и избягване на допълнителни разходи от поставяне на кратки срокове. От 9 февруари 2019 г. БСВЛ има реални шансове да работи в пълен режим и в съответствие с най-високите утвърдени стандарти в индустрията с цел безопасност на пациентите и защита на информацията.
Цитираните по-горе активности са в изпълнение на изискване на Европейската Директива за фалшивите лекарства 2011/62/ЕС и допълващите делегирани актове 2016/16. Ключов момент за функционирането на Европейската система за проследимост и верификация на лекарствата и оперативната съвместимост между отделните национални системи е използването на хармонизиран подход за маркиране на лекарствата от държавите членки. За целта се въвежда двумерния баркод GS1 Data Matrix, който кодира уникален номер на продукта (по-голямата част от държавите в Европа използват GS1 GTIN, Global Trade Item Number), сериен номер, номер на партида и срок на годност. Идентифициращата информация от 2D баркода GS1 Data Matrix, ще бъде препращана към Европейски център (EU Hub) и към Националните системи, която за България е БСВЛ. Целта на Директивата за фалшифицираните лекарства (FMD) е да предотврати навлизането на фалшиви лекарства в законната верига на доставки и повишаване безопасността на пациентите.
За повече информация, свързана с маркирането на лекарства с GS1 DataMatrix, се обърнете към GS1 България на тел.: 02/811 7 433.
Още новини:
-
27-04-2018 г.
-
26-04-2018 г.
-
26-04-2018 г.
-
25-04-2018 г.
-
24-04-2018 г.

 1 USD =
1 USD =  1 GBP =
1 GBP =  1 CHF =
1 CHF =  ISO 9001:2015
ISO 9001:2015